Técnicas inmunológicas.
1. Interacción antígeno-anticuerpo
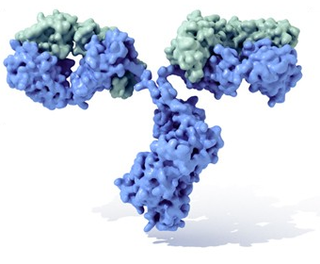
La unión antígeno-anticuerpo (Ag-Ac) es una interacción reversible en la que están involucrados enlaces no-covalentes. En la interacción in vitro de un antígeno (Ag) con su correspondiente anticuerpo (Ac) se distinguen dos etapas, la interacción primaria no visualizable y la interacción secundaria, que sigue a la anterior y se caracteriza por la aparición de un fenómeno visible como la aglutinación o la precipitación. Por otro lado, no siempre que se produce la interacción primaria Ag-Ac, se produce la interacción secundaria, ya que, para conseguir fenómenos visibles, son indispensables determinadas concentraciones y características de los Ags y Acs.

2. Interacción Secundaria Ag-Ac
Las técnicas inmunológicas que evidencian la interacción Ag-Ac a través de una reacción secundaria (precipitación o aglutinación) son, generalmente, más económicas y sencillas que aquellas que permiten visualizar la interacción primaria (ver más adelante). 2.a. Reacciones de precipitación Al mezclar cantidades suficientes de Ag soluble con Acs específicos, la interacción Ag-Ac puede dar lugar a una red capaz de ser visualizada como un precipitado. Esa red de la que hablamos, no es otra cosa que grandes complejos inmunes (CI) formados por la interacción Ag-Ac. Tal como se observa en la figura, cuando se agregan concentraciones crecientes de Ag soluble a una cantidad fija de suero conteniendo Acs específicos, a medida que la cantidad de Ag agregado aumenta, la cantidad de precipitado se incrementa hasta alcanzar un máximo, luego del cual declina. En un extremo de la curva de precipitación, cuando se agregan pequeñas cantidades de Ag, los CI se forman en exceso de Ac. En el otro extremo, al agregar grandes cantidades de Ag, los CI se forman en exceso de Ag siendo pequeños y probablemente constituidos por una molécula de Ac y dos de Ag. Entre estas dos situaciones extremas se encuentra la zona de equivalencia, en donde la relación Ag-Ac permite la formación de grandes redes de CI que precipitan.La reacción de precipitación depende de la VALENCIA del Ac y del Ag. La valencia del Ac da idea del número de sitios que posee para reconocer al Ag. De esta manera, un Ac bivalente posee dos sitios capaces de reconocer al Ag. Del mismo modo, la valencia de un Ag nos habla del máximo número de epitopes que posee. Para que se pueda producir la interacción secundaria Ag-Ag con la consecuente formación del precipitado, tanto el Ag como el Ac deben ser, al menos, bivalentes.
3. Interacción primaria Ag-Ac
Si bien la interacción primaria Ag-Ac no es visible, existen distintos métodos que hacen posible visualizarla. La estrategia consiste en "marcar" al Ac o al Ag mediante la unión covalente (conjugación) de determinadas moléculas, tales como FLUOROCROMOS, ISOTOPOS RADIOACTIVOS o ENZIMAS, para poder hacer visible esa primera interacción. Tal como se observa en la Tabla, dependiendo del marcador que se utilice, la técnica inmunológica recibe un determinado nombre y utiliza un sistema de detección diferente. Las técnicas que veremos a continuación no son tan sencillas y económicas como las que vimos anteriormente, sin embargo son mucho mas sensibles, es decir, son capaces de detectar menores concentraciones de Ag o Ac.
4. Otras técnicas

.a PROTEÍNOGRAMA ELECTROFORÉTICO El proteínograma electroforético es un técnica sencilla de laboratorio que permite separar en 5 fracciones o grupos a las proteínas presentes en un determinado fluido biológico (suero, orina, etc.). La técnica se basa en la separación electroforética de las distintas proteínas por medio de la aplicación de un campo eléctrico sobre un soporte de agarosa o acetato de celulosa. Una vez finalizada la corrida electroforética las bandas proteicas pueden ser visualizadas luego de la utilización de colorantes para proteínas. Posteriormente, las bandas que se observan a simple vista (Figura A) pueden ser cuantificadas por un densitómetro, el cual cuantifica la intensidad y anchura de cada banda (Figura B), pudiendo obtenerse los porcentajes de cada una de las 5 fracciones proteicas. Las distintas fracciones que podemos encontrar son: Albumina, alfa 1 globulinas (α1), alfa 2 globulinas (α2), beta globulinas (β) y gamma globulinas (γ).
• ALBÚMINA: es una proteína que se sintetiza en el hígado y es la de mayor concentración en el suero.
• α1: dentro de esta fracción se encuentran numerosas proteínas entre las cuales podemos mencionar a la alfa 1-antitripsina y la alfa 1-antiquimiotripsina
• α2: dentro de esta fracción se incluyen la haptoglobina y la proteína C reactiva.
• β: en esta fracción podemos encontrar, entre otras, a la fibronectina, transferrina y beta 2 microglobulina.
• γ: en esta fracción se encuentran las inmunoglobulinas, las cuales pueden disminuir en ciertas inmunodeficiencias y aumentar en ciertos procesos de inflamación crónica (artritis reumatoidea, lupus eritematoso sistémico), infecciones y alergias.
5. Técnicas de tipificación de antígenos de histocompatibilidad
1. Estudios de histocompatibilidad para transplante de órganos vascularizados
2. Estudios de histocompatibilidad para transplante de médula ósea
3. Estudios de paternidad
4. Estudios de asociación de alelos del HLA con enfermedades (susceptibilidad)
5. Estudios antropológicos para establecer posibles relaciones entre distintas poblaciones o grupos étnicos.
6. Cross match
Determinar la presencia de anticuerpos específicos contra alelos del HLA en suero de pacientes en lista de espera para transplante de órganos sólidos vascularizados. Modalidades: 6.a. Cross-match final contra dador: Tiene por objeto analizar la presencia de anticuerpos séricos dirigidos específicamente contra los alelos del HLA de un posible donante. El análisis de la presencia o ausencia de estos anticuerpos es fundamental para decidir si el transplante se realiza o no. Esto se debe a que la presencia de este tipo de anticuerpos preformados en el receptor de un transplante lleva inevitablemente a un rechazo hiperagudo. Esta técnica puede realizarse por microlinfocitotoxicidad en placas de Terasaki o citometría de flujo. En el primer caso se enfrenta suero del receptor con células de sangre periférica del posible donante (si es donante vivo) o con células de bazo o ganglio linfático (si es donante cadavérico). Luego de una etapa de incubación, se agrega fuente de complemento y se prosigue con la técnica tal como se describió en "Microlinfocitotoxicidad en placas de Terasaki". En el caso del cross-match final contra dador por citometría de flujo, se enfrentan células mononucleares de sangre periférica o de bazo o ganglio linfático del posible donante, con suero del receptor. Luego de una incubación, se revela el sistema con inmunoglobulinas de cabra o conejo anti-inmunoglobulinas humanas, marcadas con fluorocromos (en general se emplea isotiocianato de fluoresceína). Finalmente, se analizan las células en un citómetro de flujo.